Phương pháp trao đổi ion được sử dụng rộng rãi trong các quá trình xử lý nước thải cũng như nước cấp.
Trong xử lý nước cấp, phương pháp này thường được sử dụng để khử các muối, khử cứng, khử khoáng, khử màu, khử kim loại, các ion kim loại nặng và các ion kim loại có trong nước.
Trong xử lý nước thải, phương pháp trao đổi ion được sử dụng để loại ra khỏi nước các kim loại (kẽm, đồng, crom, chì, thủy ngân….), các hợp chất của asen, photpho, xianua và các chất phóng xạ. Phương pháp này cho phép thu hồi các chất có giá trị với độ làm sạch nước cao.
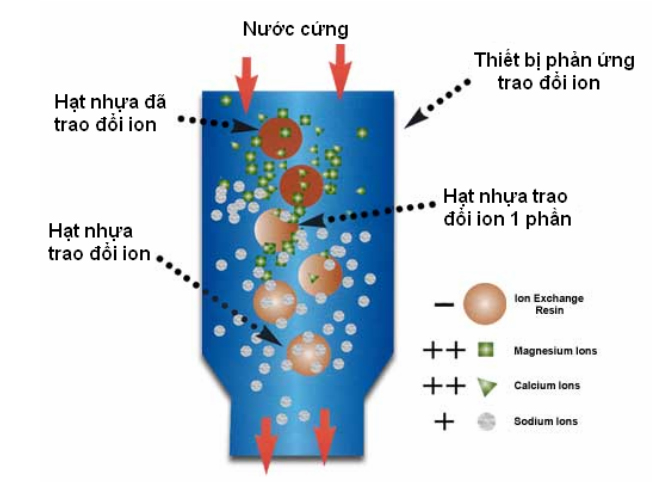
1. Cơ sở của phương pháp:
Là quá trình trao đổi ion gồm các phản ứng hóa học đổi chỗ (phản ứng thế) giữa các ion trong pha lỏng và các ion trong pha rắn (là nhựa trao đổi). Qúa trình này phụ thuộc vào từng loại nhựa trao đổi và các loại ion khác nhau.
Có hai phương pháp sử dụng trao đổi ion với lớp nhựa chuyển động, vận hành và tái sinh liên tục; và trao đổi ion với lớp nhựa trao đổi đứng yên, vận hành và tái sinh gián đoạn. Trong đó trao đổi ion với lớp nhựa tĩnh là phổ biến nhất.
2. Phân loại vật liệu trao đổi ion:
– Lọai cationit
a. Vô cơ
Tự nhiên (zeolit, khoáng sét).
Tổng hợp (zeolit tổng hợp, permulit, silicat tổng hợp).
b. Hữu cơ
Tự nhiên (than bùn, ligin).
Than sunfon hóa.
Tổng hợp (nhựa trao đổi ion trên cơ sở phản ứng trùng ngưng polymer hóa).
– Loại anionit
a. Vô cơ
Tự nhiên (dolomite, apatit, hydroxyl apatit).
Tổng hợp (silicat của kim loại nặng).
b. Hữu cơ
Tổng hợp (nhựa trao đổi ion).
3. Tính năng thuận nghịch của phản ứng trao đổi ion:
Phản ứng trao đổi ion là phản ứng thuận nghịch. Dựa trên tính chất này người ta dùng dung dịch chất hoàn nguyên, thông qua chất trao đổi ion đã mất hiệu lực để khôi phục năng lực trao đổi của nó.
4. Tính acid, kiềm:
Tính năng của chất Cationit RH và chất Anionit ROH, giống chất điện giải acid, kiềm.
5. Tính trung hòa và thủy phân:
Tính năng trung hòa và thủy phân của chất trao đổi ion giống chất điện giải thông thường.
6. Tính chọn lựa của chất trao đổi ion:
Ở hàm lượng ion thấp trong dung dich, nhiệt độ bình thường, khả năng trao đổi tăng hóa trị của ion trao đổi tăng.
7. Xử lý các chất độc hại trong nước bằng phương pháp trao đổi ion
Xử lý amoni (NH4+) trong nước ngầm.
Nghiên cứu xử lý amoni trong nước ngầm ứng dụng kỹ thuật trao đổi ion trên vật liệu trao đổi ion là nhựa cationit; các yếu tố ảnh hưởng đến quá trình trao đổi amoni là nồng độ amoni trong nước đầu vào, tốc độ dòng chảy, độ cứng của nước và thời gian hoàn nguyên…
Khử sắt trong nước ngầm.
Trong nước ngầm sắt thường tồn tại ở dạng ion, sắt có hóa trị 2 (Fe 2+) là thành phần của các muôí hòa tan, hàm lượng sắt có trong các nguồn nước ngầm thường cao và phân bố không đồng đều trong các lớp trầm tích dưới đất sâu. Nước có hàm lượng sắt cao, làm cho nước có mùi tanh và có màu vàng, gây ảnh hưởng không tốt đến chất lượng nước ăn uống sinh hoạt và sản xuất. Do đó, khi mà nước có hàm lượng sắt cao hơn giới hạn cho phép theo tiêu chuẩn thì chúng ta phải tiến hành khử sắt.
Fe(OH)3, FeCl3…trong đó Fe(OH)3 là chất keo tụ, dễ dàng lắng đọng trong các bể lắng và bể lọc. Vì thế,các hợp chất vô cơ của sắt hòa tan trong nước hoàn toàn có thể xử lý bằng phương pháp lý học: làm thoáng lấy oxy của không khí để oxy hóa sắt hóa trị 2 thành sắt hóa trị 3 và cho quá trình thủy phân, keo tụ Fe(OH) xảy ra hoàn toàn trong các bể lắng, bể lọc tiếp xúc và các bể lọc.
Áp dụng quá trình khử sắt vào việc xử lý nước ngầm để cấp nước cho cộng đồng dân cư nông thôn.
Mục đích của việc xử lý nước cấp là cung cấp đầy đủ lượng nước cho quá trình sử dụng của người dân và đảm bảo an toàn về mặt hóa học. Nước có chất lượng tốt không chứa các chất gây đục, gây ra màu, mùi, vị của nước. Tóm lại, mọi nguồn nước thô sau khi qua hệ thống xử lý phải đạt: “tiêu chuẩn vệ sinh đối với chất lượng nước cấp cho ăn uống và sinh hoạt – TCVN 5501 – 1991”.
Bùn hoạt tính trong xử lý nước thải
Phương thức cấp khí cho các dạng bể aeroten trong xử lý nước thải
Oxi hóa các chất hữu cơ của ozone
Hệ thống xử lý nước cứng
Phương pháp ion trong xử lý nước cấp
